FÍSICAMENTE: Desde el punto de vista físico, el agua circula constantemente en un ciclo de evaporación o transpiración (evapotranspiración), precipitación, y desplazamiento hacia el mar. Los vientos transportan tanto vapor de agua como el que se vierte en los mares mediante su curso sobre la tierra, en una cantidad aproximada de 45.000 km³ al año. En tierra firme, la evaporación y transpiración contribuyen con 74.000 km³ anuales al causar precipitaciones de 119.000 km³ cada año.
QUÍMICAMENTE: casi la totalidad de los procesos químicos que ocurren en la naturaleza, 831 como los que se realizan en el laboratorio, tiene lugar entre sustancias disueltas esto entre soluciones acuosas. Su fórmula química es H2O, protóxido de hidrogeno formado al combinarse dos volúmenes de hidrogeno por uno de oxígeno, se presenta en la naturaleza en estado sólido como el hielo, nieve, escarcha y neviza, Liquido en lluvias, mares etc., .gaseoso en vapor de agua. el agua se trata de un compuesto extremadamente complejo (hay que tener en cuenta los isótopos del hidrógeno y del oxígeno) y del que, en la actualidad, no se puede tener una idea clara sobre su naturaleza y sus agrupaciones moleculares. Además es un compuesto polar, lo que hace que todas sus constantes físicas sean anormales.
BIOLOGICAMENTE: Es esencial para la supervivencia de todas las formas conocidas de vida. El término agua, generalmente, se refiere a la sustancia en su estado líquido, pero la misma puede hallarse en su forma sólida llamada hielo, y en forma gaseosa denominada vapor. El agua cubre el 71% de la superficie de la corteza terrestre.2 Se localiza principalmente en los océanos donde se concentra el 96,5% del agua total, los glaciares y casquetes polares poseen el 1,74%, los depósitos subterráneos (acuíferos), los permafrost y los glaciares continentales suponen el 1,72% y el restante 0,04% se reparte en orden decreciente entre lagos.
2. ESTRUCTURA DEL AGUA , PUENTES DE HIDROGENO , POLARIDAD DE AGUA.
La configuración más común de las moléculas de agua líquida es tetraédrica con dos átomos de hidrógeno unidos covalentemente al oxígeno y otros dos hidrógenos unidos por enlaces de hidrógeno. Ya que los enlaces de hidrógeno varían en longitud muchas de estas moléculas de agua no son simétricas y forma tetraedros irregulares transitorios entre sus cuatro átomos de hidrógeno asociados.2 Cuando la molécula de
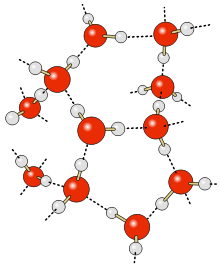
Los puentes de Hidrógeno, se forman por átomos de Hidrógeno localizados entre átomos electronegativos. La estructura del agua favorece las interacciones para formar puentes de Hidrógeno, el arreglo siempre es perpendicular entre las moléculas participantes, además, es favorecido por que cada protón unido a un Oxígeno muy electronegativo encuentra un electrón no compartido con el que interactúa uno a uno. De lo anterior se concluye que cada átomo d Oxígeno en el agua interacciona con 4 protones, dos de ellos unidos covalentemente y dos a través de puentes de Hidrógeno.
La polaridad química o solo polaridad es una propiedad de las moléculas que representa la separación de las cargas eléctricas en la misma. Esta propiedad está íntimamente relacionada con otras propiedades como la solubilidad, punto de fusión, punto de ebullición, fuerzas intermoleculares, etc.
Al formarse una molécula de modo covalente el par de electrones tiende a desplazarse hacia el átomo que tiene mayor electronegatividad. Esto origina una densidad de carga desigual entre los núcleos que forman el enlace (se forma un dipolo eléctrico). El enlace es más polar cuanto mayor sea la diferencia entre las electronegatividades de los átomos que se enlazan; así pues, dos átomos iguales atraerán al par de electrones covalente con la misma fuerza (establecida por la Ley de Coulomb) y los electrones permanecerán en el centro haciendo que el enlace sea apolar.
3. CLASES DE AGUA
Agua dulce
Agua dura
Agua blanda
Aguas negras
Aguas grises
Aguas residuales
Aguas residuales municipales
Agua bruta
Aguas muertas
Agua alcalina
Agua capilar
Agua de adhesión
Agua de desborde
Agua de formación
Agua de gravedad
Agua de suelo
Agua disfórica
Agua estancada
Agua fósil
Agua freática
Agua funicular
Agua primitiva
Agua magmática
Agua metamórfica
Agua vadosa
Agua subterranea
El agua según sus propiedades para el consumo se divide en potable y no potable.
Según la cantidad de minerales se la considera dura o blanda.
Según la procedencia puede ser superficial o subterranea
Las aguas embotelladas suelen proceder de manantiales ricos en minerales de ahí que se la conozco, en general, como agua mineral.
4. flujogramas
4.1
1. adicionar sulfato de aluminio para disolver los bicarbonatos
2. filtrar a traves de filtros especiales que retienen las particulas en suspension
3. Purificar Para destruir las bacterias se utilizan reactivos químicos, el más común es el cloro.
4.Aeriar. el agua que ha pasado por su etapa de purificación química,pasar por estanques especiales para que se ponga en contacto con el aire y el sol que le destruyen las bacterias que aún contenga.
5.Destilar El agua con el fin de purificar el agua,que contiene cantidades de sustancias en disolución;Consiste en evaporar el agua y luego condensarla.
6.Ablandar el aguas, eliminar de sales de magnesio y de calcio. por medio de la ebullición fácilmente precipitan los carbonatos de modo que se pueden retirar estas sustancias.
4.2
1.TOMA DEL RIO. Punto de captación de las aguas; REJA. Impide la penetración de elementos de gran tamaño (ramas, troncos, peces, etc.).
2.DESARENADOR. Sedimenta arenas que van suspendidas para evitar dañar las bombas.
BOMBEO DE BAJA (Bombas también llamadas de baja presión). Toman el agua directamente de un río, lago o embalse, enviando el agua cruda a la cámara de mezcla.
3.CAMARA DE MEZCLA. Donde se agrega al agua productos químicos. Los principales son los coagulantes (sulfato de alúmina), alcalinizantes
4.DECANTADOR. El agua llega velozmente a una pileta muy amplia donde se aquieta, permitiendo que se depositen las impurezas en el fondo. Para acelerar esta operación, se le agrega al agua coagulante que atrapan las impurezas formando pesados coágulos. El agua sale muy clarificada y junto con la suciedad quedan gran parte de las bacterias que contenía.
5.FILTRO. El agua decantada llega hasta un filtro donde pasa a través de sucesivas capas de arena de distinto grosor. Sale prácticamente potable.
6.DESINFECCIÓN. Para asegurar aún más la potabilidad del agua, se le agrega cloro que elimina el exceso de bacterias y lo que es muy importante, su desarrollo en el recorrido hasta las viviendas.
7.BOMBEO DE ALTA. Toma el agua del depósito de la ciudad.
8.TANQUE DE RESERVA. Desde donde se distribuye a toda la ciudad.Muestras tomadas en distintos lugares del sistema.
9.CONTROL FINAL. Antes de llegar al consumo, el agua es severamente controlada por químicos expertos, que analizan
CONCLUSIONES
Creo que debemos tomar conciencia ah tiempo antes de que el agua empieze ah escasear pues todos sabemos que al empezar ah acabarse empezaremos ah preocuparnos y ya sera demasiado tarde para poder hacer algo y sin agua no hay vida asi que tenemos que hacer algo para que el agua SUBSISTA.





